Phenolrot
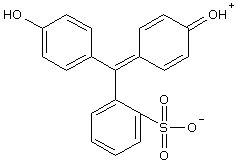
Strukturformel
Bemerkungen
- Von gelb nach rot umschlagender pH-Indikator mit einem Umschlagintervall von ca. 6,4 bis 8,0 aus der Gruppe der Sulfophthaleine.
- Das Molekül liegt ist als Festsubstanz und in stark saurer Lösung (< pH 0) wie oben abgebildet als Zwitterion vor. Nur so ist seine rote Farbe zu erklären.
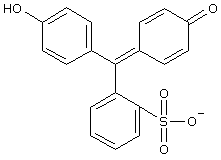
- In normal saurer Lösung liegt die einfach deprotonierte Form vor, die gelb erscheint. Die hypsochrome Verschiebung ergibt sich, da nun keine vorgegebene Ladung mehr im für die Farbe verantwortlichen konjugierten System mehr vorliegt:
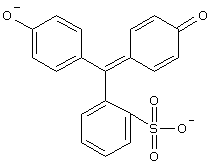
- Wird diese einfach deprotonierte Form ein weiteres mal deprotoniert, so schlägt die Farbe wieder ins Rot-Violette um:
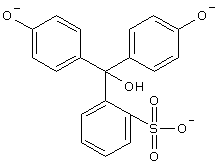
- Im stark Basischen (> pH 14) kann eine weitere Deprotonierung stattfinden. Das sich ergebende Trianion ist farblos: