pH-Wert
Definition
- Der pH-Wert ist der negative dekadische
Logarithmus der Aktivität der Wasserstoff-Ionen einer Lösung
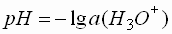
Bemerkungen
- Da die Aktivität a
eines Stoffes meist nur
schlecht berechnet werden kann, wird statt ihrer oftmals die Konzentration
c
verwendet. In stark verdünnten Lösungen sind Aktivität und
Konzentration nahezu gleich, mit steigender Konzentration bewegen sie sich
jedoch zunehmend auseinander.
- Neben dem pH-Wert kann auch der pOH-Wert
bestimmt werden, der die Konzentration der OH--Ionen in Form des negativen
dekadischen Logarithmus ausdrückt.
- Zwischen pH- und pOH-Wert besteht in
wässriger Lösung folgender Zusammenhang (bei 25 °C):
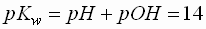
- Der pH-Wert ist abhängig von
- der Konzentration der Lösung
- der Stärke der Protolyte
- der Autoprotolyse des Wassers
|
