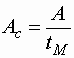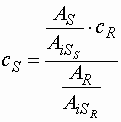Kapillarelektrophorese
Synonym
Aufbau
- Die verwendeten Spannungen in der CE betragen zwischen 100 - 30.000 V bei Stromstärken zwischen 10 µA und 10 mA.
- Die Kapillaren bestehen aus Quarz und weisen Durchmesser von 5 - 200 µm auf, wobei meist 50 - 100 µm dicke Kapillaren eingesetzt werden.
- Die Länge der eingesetzten Kapillaren beträgt 10 - 100 cm.
- Aufgrund der relativ großen fließenden Ströme müssen die Kapillaren thermostatisiert werden.
- Zum Schutz der empfindlichen Kapillaren sind sie meist mit einem Polymermantel beschichtet, der an der Detektionsstelle jedoch unterbrochen sein muss.
- Die dort verwendeten Detektionsverfahren entsprechen weitgehend denen in der HPLC, wiederum mit dem Schwerpunkt der spektrometrischen Verfahren.
- Die Grundlösungen sind meist wässrig.
- Die Probenaufgabe kann auf verschiedene Arten erfolgen, z.B.
- hydrostatisch
- Durch Ausnutzung der Höhendifferenz zwischen Inlet und Outlet.
- hydrodynamisch
- Durch Druck oder Vakuum wird die Probelösung in die Kapillare gepresst bzw. gesaugt.
- elektrokinetisch
- Durch kurzzeitiges Anlegen einer Spannung wandert die Probe in die Kapillare. Dies ist jedoch oftmals problematisch da so beim Auftragen der Probe Bestandteile mit höherer Ionenleitfähigkeit in höherer
Konzentration als solche mit niedrigerer Ionenleitfähigkeit in die Kapillare gelangen.
Trennverfahren
- Kapillarzonenelektrophorese (CZE)
- Die CZE ist das einfachste und am häufigsten eingesetzte Verfahren der CE.
- Puffer, pH-Wert und Feldstärke sind über die Trennstrecke konstant.
- Die Trennung der Probenbestandteile erfolgt durch deren
unterschiedliche Mobilitäten.
- Eine Beeinflussung der Selektivität / Trennleistung ist möglich über:
- pH-Wert und Zusammensetzung des Puffers (Stabilität, Mobilität, Ionenstärke)
- Kapillarlänge, Durchmesser, Charge
- Spannung / Feldstärke
- organische Modifier (Leitfähigkeit, Solvatation, pKa-Werte, elektroosmotischen Fluss)
- Probenvorbereitung und -aufgabe (Lösemittel, Injektionszeit, Ionenstärke)
- Temperatur
- Mizellare Elektrokinetische Chromatographie (MEKC)
- Unter Einsatz von Tensiden (Konzentration > CMC -> Bildung von Mizellen) ermöglicht die MEKC die Auftrennung ungeladener Substanzen.
- Durch die unterschiedlichen Aufenthaltswahrscheinlichkeiten der
Probenbestandteile in der wässrigen mobilen und der pseudo-stationären Phase wird die effektive Wanderungsgeschwindigkeit beeinflusst.
- Pseudo-stationär, da die Nettobewegungen der sich um die Kationen bildenden Mizellen aus den negativ geladenen Tensid-Molekülen stark verlangsamt sind
- Eingesetztes Tensid ist meist SDS.
- Kapillargelelektrophorese (CGE)
- Da Biopolymere überwiegend als Polyanionen mit gleicher Ladungsdichte vorliegen, ist eine Auftrennung im elektrischen Feld ohne weitere Hilfsmittel nicht möglich.
Allerdings unterscheiden sich Biopolymere in
ihrer Größe, so dass eine Trennung durch Einsatz eines Geles mit restriktiven Eigenschaften möglich wird.
- Kleinere Moleküle erscheinen somit vor größeren Molekülen am Detektor.
- Als Matrices werden hauptsächlich Acrylamide, Agarose und Cellulose eingesetzt.
- Es muss bei ausgeschaltetem elektroosmotischen Fluss
gearbeitet werden.
- Haupteinsatzgebiete der CGE sind die Trennung von Makromolekülen, wie DNA und von mit SDS denaturierten Proteinen.
- Der EOF sollte möglichst klein gehalten werden, damit nicht das Gel selbst wandert.
- Isoelektrische Fokussierung in Kapillaren (CIEF)
- Zwitterionische und amphotere Proben, die sich nicht in ihrer Mobilität, aber in ihren isoelektrischen Punkten
unterscheiden, können mit Hilfe eines pH-Gradienten in der Kapillare getrennt werden.
- Der elektroosmotische
Fluss
muss
hierbei unterdrückt werden, um die Ampholytlösung, die der Ausbildung des pH-Gradienten dient, nicht aus der Kapillare herauszuspülen.
- Isotachophorese in Kapillaren (CITP)
- Wegen Detektionsproblemen und der Schwierigkeit geeignete Leit- und Folgeelektrolyte sowie Spacerionen zu finden erlangte dieses Verfahren keine analytische Bedeutung.
- Dagegen findet die ITP Anwendung als
Anreicherungsschritt vor der eigentlichen CE-Trennung (Probenkonzentrierung).
- Kapillar-Elektrochromatographie (CEC)
- Die CEC vereint Vorteile der CE und der HPLC.
- Es werden gepackte Kapillaren eingesetzt, die mit Materialien aus der HPLC
befüllt sind.
- Zum
elektroosmotischen Fluss
tragen sowohl die Ladungen der Kapillarwand, als auch die des Füllmaterials bei.
- Die Trennung erfolgt durch unterschiedliche Wechselwirkung der Probenbestandteile mit der stationären Phase und unterschiedliche
elektrophoretische Migration; der Transport zum Detektor erfolgt durch die Eigenmobilität der Probe und / oder den elektroosmotischen Fluss.
Enantiomerentrennung
- Der Zusatz von chiralen Selektoren als Pufferadditiva macht eine Trennung von Enantiomeren in der CE möglich.
- Die unterschiedliche Affinität der Enantiomere
zu den im Puffer gelösten chiralen Selektoren bewirkt
Unterschiede in den elektrophoretischen Mobilitäten.
- Die Trennung von geladenen Analyten erfolgt hauptsächlich mit ungeladenen Selektoren oder Selektoren entgegengesetzter Ladung und die von ungeladenen Analyten mit geladenen Selektoren.
- Als chirale Selektoren kommen u.a. zum Einsatz
- Cyclodextrine
- native Cyclodextrine (6,7 oder 8
a-1,4-glycosidisch verknüpfte Glucoseeinheiten)
- chemisch modifizierte Cyclodextrine
- chirale Kronether
- chirale Mizellbildung
- Die Auffindung des geeigneten Selektors erfolgt empirisch.
- Die Optimierung der Methode erfolgt über den pH-Wert und die Selektorkonzentration.
- Im Gegensatz zur Flüssigkeitschromatographie
sind keine teuren Spezialsäulen notwendig und
der Verbrauch an chiralem Selektor ist durch die Verwendung der sehr dünnen Kapillaren nur gering.
Quantitative Bestimmungen
- Der Zusatz von internem Standard und Referenzsubstanz ist notwendig. Die Auswertung erfolgt über die mit der Migrationszeit korrigierten Peakflächen
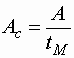
| Ac |
: |
korrigierte Peakfläche |
| A |
: |
Peakfläche |
| tM |
: |
Migrationszeit |
- oder über die Peakflächenverhältnisse von Probe zur Referenz, beide korrigiert mit dem jeweiligen internen Standard
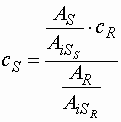
| cS |
: |
Konzentration der Probe |
| AS |
: |
Fläche der Probe |
| AiSS |
: |
Fläche des internen Standards bei der Probe |
| cR |
: |
Konzentration der Referenz |
| AR |
: |
Fläche der Referenz |
| AiSR |
: |
Fläche des internen Standards bei der Referenz |
EOF
- Ist die Abkürzung für Endo-Elektroosmotischer Fluss
- Er entsteht pH-abhängig beim Einsatz von Quarzkapillaren durch die Deprotonierung von Silanolgruppen an deren Oberfläche. An die nun negativ geladene Kapillarwand lagern sich Kationen aus der Lösung an, die im
elektrischen Feld zur Kathode wandern. Aufgrund der Clusterstruktur des Wassers wird dabei die gesamte Flüssigkeitssäule in der Kapillare mitgerissen.
- Neutrale Teilchen wandern mit dem EOF
- Kationen wandern schneller als der EOF, da hier der zur Kathode gerichtete EOF durch die Ladung Kations verstärkt wird.
- Anionen wandern langsamer als der EOF, da die negative Ladung für eine gegen den EOF gerichtete Kraft sorgt.
- Der EOF kann durch Tenside, z.B. Ammoniumsalze oder Pyridiniumsalze beeinflusst werden.
- Bei der MEKC wandern "polarere" Neutralteilchen schneller als "unpolare".
Strömungsprofile
- Das bessere Strömungsprofil der CE ist einer der Hauptgründe für die deutlich kleineren Peakbreiten gegenüber der HPLC
und damit die höhere Genauigkeit (bei dennoch meist höherer Geschwindigkeit).
Bemerkungen
- Die Selektivität lässt sich bei vielen Substanzen über den pH-Wert deutlich erhöhen.
- Als EOF-Marker wird meist Acetanilid
eingesetzt.
- Problematisch ist die Abhängigkeit der Peakbreite vom elektro-endoosmotischen Fluss (EOF), der sich auch u.U. zwischen mehreren Messungen in der gleichen Kapillare ändern kann. Aus diesem Grund muss die Kapillare
zwischen den Messungen gut von anhaftenden Kationen befreit werden. Dazu wird eine alkoholische (Isopropanol) Pufferlösung mit SDS-Beimischung verwendet, die zwar nicht alle Rückstände bereinigt, jedoch zu gut reproduzierbaren Ergebnissen führt.
- Die Detektion kann bei stark unterschiedlichen Geschwindigkeiten der einzelnen Probenbestandteile problematisch sein, da Stoffe mit niedrigerer Geschwindigkeit länger vor dem Detektorfenster bleiben, als solche mit
höherer Geschwindigkeit. Damit liefert eine geringere Menge der langsameren Substanz einen gleich großen Peak, wie eine höhere Menge einer schnelleren.
- Das Verfahren ist gut automatisierbar.
Leistungsbewertung
- Sehr gute Trennleistungen. Es können mehr als 10 Peaks pro Minute getrennt werden, bei theoretischen Trennbodenzahlen von > 400.000.
- In der Kapillarelektrophorese kommt es zu keiner Peakverbreiterung.
- Die Präzision liegt mit 1 - 2 % relativer Standardabweichung etwas unter der der HPLC, allerdings ist die Richtigkeit höher, da die Selektivität größer ist
|